Clerodin是庞大的克罗烷(Clerodane)二萜家族(包含超过1300个成员)中首个被分离鉴定的分子。该分子早在1936年便被分离出来,但其结构的最终确定则要等到1961年,由Barton教授课题组完成。Clerodin具有很强的昆虫拒食活性,近期研究还发现其在抗癌和抗菌方面同样表现出突出活性。由于其结构极其复杂——包括7个连续的手性中心、一个不稳定的四氢呋喃并二氢呋喃侧链,以及在反式十氢萘环母核骨架上难以引入的C19位氧化态——该分子在被结构鉴定后的60多年里,始终未有成功的全合成报道。
近日,兰州大学天然产物化学全国重点实验室阳铭教授课题组成功实现了Clerodin的首次不对称全合成。他们采用模块化合成策略,将目标分子拆分位两个关键片段:一个是包含全部7个连续手性中心且C19位氧化的反式十氢萘环母核模块,另一个是侧链模块。通过这种策略,将“高氧化态、多手性中心碳骨架的合成”与“敏感杂环体系的构建”两大核心挑战拆分到不同合成阶段,从而兼顾了合成路线的效率与稳健性。

图一 Clerodin的逆合成分析
该课题组延续了其先前发展的“从尾至头”环化策略(Nat. Commun. 2022, 13, 6633),利用内烯烃甲基氧化的环氧烯炔化合物的Ti(III)催化开环氧烯炔环化反应构建C19位氧化的反式十氢萘环骨架。随后,他们通过引入C8位甲基并进行氧化态调整,最终合成了所需的母核模块。在获得母核模块后,作者利用MacMillan课题组发展的光氧化还原促进的醇的脱氧偶联引入呋喃结构,随后经双键还原和酸催化环化,完成了Clerodin的水合产物——天然产物Scutecyprol A的首次不对称全合成。最后,通过Scutecyprol A中的半缩醛进行酯化,并利用SmI2促进的缩醛的消除反应,成功构建了不稳定的四氢呋喃并二氢呋喃侧链,最终实现了Clerodin的首次不对称全合成。
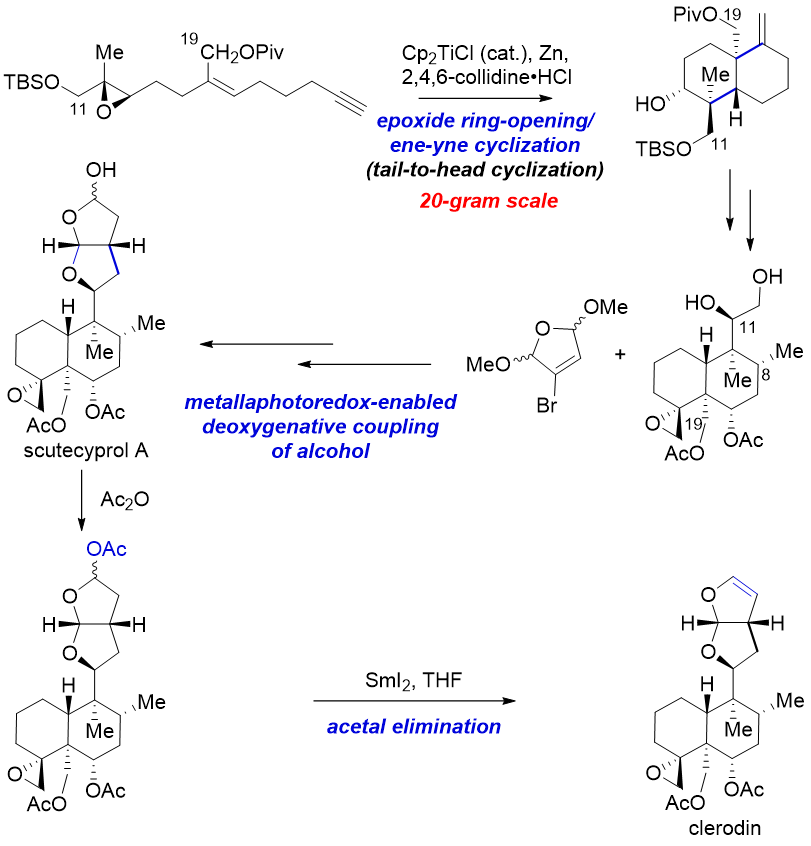
图二 Clerodin和Scutecyprol A的合成
相关研究成果近期发表在Angew. Chem. Int. Ed. (doi: org/10.1002/anie.202515206)上。兰州大学博士研究生殷其爽为论文第一作者,硕士研究生党煜、硕士研究生冯思远、博士研究生张泽强、硕士研究生屠原铭对此项研究做出了重要贡献,通讯作者为兰州大学天然产物化学全国重点实验室阳铭教授。
该工作受到国家自然科学基金,甘肃省科技厅,中央高校基本科研业务费和“文魁基金”的大力资助。